Comment fonctionnent les protéines ? Les protéines sont un élément structural essentiel et irremplaçable, indispensable à la croissance ainsi qu’au métabolisme de l’organisme humain et de tous les êtres vivants.2 photos
Les grandes molécules de protéines sont composées de composants plus petits : les acides aminés, et ont souvent une structure très complexe.
Les protéines de diverses natures jouent un rôle extrêmement important dans l’organisme humain. Les protéines structurales des tissus conjonctifs contiennent du collagène, celles de la peau du kératine, les muscles contiennent de l’actine et de la myosine, tandis que les protéines cellulaires sont liées au tubuline. D’autres protéines sont des enzymes qui accélèrent les réactions chimiques à l’intérieur des cellules, des hormones et des anticorps : des protéines impliquées dans la protection de l’organisme contre les influences nocives et les maladies. Les protéines sanguines, telles que l’hémoglobine et l’albumine, sont responsables de la coagulation du sang, uniquement lorsque c’est nécessaire, par exemple en cas de blessure.
Les acides aminés constituent les unités structurelles de base. Comme tous les substances organiques, les molécules protéiques sont composées d’atomes de carbone, d’hydrogène et d’oxygène. De plus, les protéines contiennent de l’azote et, dans de nombreux cas, du soufre. L’unité structurelle de base d’une molécule protéique est l’acide aminé. Environ 20 types d’acides aminés sont connus, qui peuvent se combiner entre eux pour former un grand nombre de différentes combinaisons. Certaines acides aminés peuvent être synthétisées dans l’organisme, tandis que d’autres ne proviennent que de l’environnement extérieur. Pour maintenir sa santé, l’homme doit consommer au moins 30 grammes de protéines par jour.
La structure fondamentale d’une molécule d’acide aminé est composée d’une chaîne d’atomes de carbone. Aux extrémités de la molécule se trouvent deux groupes chimiques différents : d’un côté, un groupe amino, et de l’autre, un restant d’acide carboxylique. Le groupe amino d’un acide aminé peut interagir avec le groupe acidique du groupe amino d'un autre acide aminé, avec libération d’une molécule d’eau. Ce processus est à l’origine de la formation de longues chaînes d’acides aminés.
La structure de l’acide aminé détermine sa solubilité dans l’eau, ainsi que ses propriétés amphotères : sa capacité à agir à la fois en tant qu’acide et en tant que base. Cela permet à une molécule de protéine d’exister à la fois dans un milieu acide et dans un milieu alcalin. Les acides aminées possèdent également des propriétés tampons, ce qui est d’une grande importance pour l’homéostasie, c’est-à-d régulation du maintien de la stabilité de l’environnement interne de l’organisme.
La matrice pour la formation d’une molécule de protéine est la séquence d’ADN. Dans la cellule, la synthèse des chaînes d’acides aminés a lieu sur les ribosomes, avec l’aide de l’acide nucléique RNA.
La structure primaire d’une molécule de protine est déterminée par la séquence des acides aminés assemblés sur les ribosomes. L’ordre de cette assembly dépend, à son tour, de la séquence d’ADN. Cette structure primaire constitue le cadre de base de la molécule de protéine.
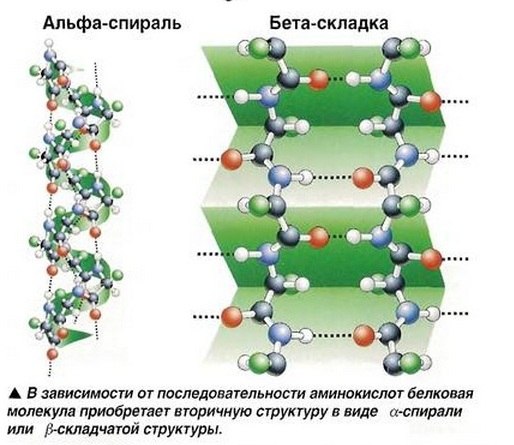
Une fois que une longue chaîne polypeptidique a été formée, elle commence à prendre une structure tridimensionnelle complexe, bien qu’elle reste parfois encore sous forme de simple chaîne d’acides amines. Le processus de formation de la structure secondaire se produit grâce à l’établissement de liaisons hydrogène, qui, bien qu’étant assez faibles, sont suffisamment fortes pour maintenir la forme particulière de la protéine. Les atomes d’hydrogène interagissent avec des atomes spécifiques à l’intérieur de la chaîe pour former deux types de structures secondaires : les structures en hélice α, qui tournent à droite, et les structures en pli β, qui sont plates. Dans certaines molécules de protéines, on peut observer une alternance de ces deux types de structures secondaires sur différentes parties de la chaîe.
Une protéine ayant une très longue chaire polypeptidique peut présenter en plus une structure troisièmeaire et une structure quatrièmeaire.
Under normal conditions, proteins are relatively stable. Their activity is determined by their three-dimensional structure and the bonds that hold the molecules together. However, these interatomic bonds are sensitive to factors such as increased acidity and temperature. The process by which a protein loses its three-dimensional structure is called denaturation. In some cases, this process can be reversible. If the changes in pH or temperature reach extreme values, the process becomes irreversible.
Les protéines de diverses natures jouent un rôle extrêmement important dans l’organisme humain. Les protéines structurales des tissus conjonctifs contiennent du collagène, celles de la peau du kératine, les muscles contiennent de l’actine et de la myosine, tandis que les protéines cellulaires sont liées au tubuline. D’autres protéines sont des enzymes qui accélèrent les réactions chimiques à l’intérieur des cellules, des hormones et des anticorps : des protéines impliquées dans la protection de l’organisme contre les influences nocives et les maladies. Les protéines sanguines, telles que l’hémoglobine et l’albumine, sont responsables de la coagulation du sang, uniquement lorsque c’est nécessaire, par exemple en cas de blessure.
Les acides aminés constituent les unités structurelles de base. Comme tous les substances organiques, les molécules protéiques sont composées d’atomes de carbone, d’hydrogène et d’oxygène. De plus, les protéines contiennent de l’azote et, dans de nombreux cas, du soufre. L’unité structurelle de base d’une molécule protéique est l’acide aminé. Environ 20 types d’acides aminés sont connus, qui peuvent se combiner entre eux pour former un grand nombre de différentes combinaisons. Certaines acides aminés peuvent être synthétisées dans l’organisme, tandis que d’autres ne proviennent que de l’environnement extérieur. Pour maintenir sa santé, l’homme doit consommer au moins 30 grammes de protéines par jour.
La structure fondamentale d’une molécule d’acide aminé est composée d’une chaîne d’atomes de carbone. Aux extrémités de la molécule se trouvent deux groupes chimiques différents : d’un côté, un groupe amino, et de l’autre, un restant d’acide carboxylique. Le groupe amino d’un acide aminé peut interagir avec le groupe acidique du groupe amino d'un autre acide aminé, avec libération d’une molécule d’eau. Ce processus est à l’origine de la formation de longues chaînes d’acides aminés.
La structure de l’acide aminé détermine sa solubilité dans l’eau, ainsi que ses propriétés amphotères : sa capacité à agir à la fois en tant qu’acide et en tant que base. Cela permet à une molécule de protéine d’exister à la fois dans un milieu acide et dans un milieu alcalin. Les acides aminées possèdent également des propriétés tampons, ce qui est d’une grande importance pour l’homéostasie, c’est-à-d régulation du maintien de la stabilité de l’environnement interne de l’organisme.
La matrice pour la formation d’une molécule de protéine est la séquence d’ADN. Dans la cellule, la synthèse des chaînes d’acides aminés a lieu sur les ribosomes, avec l’aide de l’acide nucléique RNA.
La structure primaire d’une molécule de protine est déterminée par la séquence des acides aminés assemblés sur les ribosomes. L’ordre de cette assembly dépend, à son tour, de la séquence d’ADN. Cette structure primaire constitue le cadre de base de la molécule de protéine.
Une fois que une longue chaîne polypeptidique a été formée, elle commence à prendre une structure tridimensionnelle complexe, bien qu’elle reste parfois encore sous forme de simple chaîne d’acides amines. Le processus de formation de la structure secondaire se produit grâce à l’établissement de liaisons hydrogène, qui, bien qu’étant assez faibles, sont suffisamment fortes pour maintenir la forme particulière de la protéine. Les atomes d’hydrogène interagissent avec des atomes spécifiques à l’intérieur de la chaîe pour former deux types de structures secondaires : les structures en hélice α, qui tournent à droite, et les structures en pli β, qui sont plates. Dans certaines molécules de protéines, on peut observer une alternance de ces deux types de structures secondaires sur différentes parties de la chaîe.
Une protéine ayant une très longue chaire polypeptidique peut présenter en plus une structure troisièmeaire et une structure quatrièmeaire.
Under normal conditions, proteins are relatively stable. Their activity is determined by their three-dimensional structure and the bonds that hold the molecules together. However, these interatomic bonds are sensitive to factors such as increased acidity and temperature. The process by which a protein loses its three-dimensional structure is called denaturation. In some cases, this process can be reversible. If the changes in pH or temperature reach extreme values, the process becomes irreversible.

Trouvez les meilleurs professionnels pour votre projet
Des spécialistes en réparation, construction et rénovation prêts à vous aider
Galeries recommandées

Olga Gourieva est née le 18 novembre 1980 dans la ville de Iaroslavl.
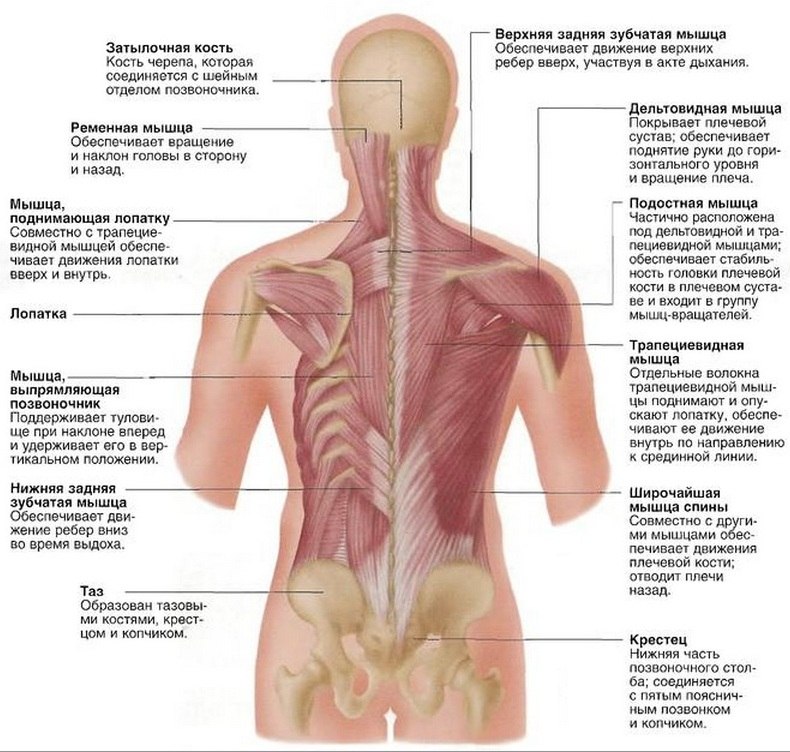
Les muscles du dos. Les muscles du dos nous permettent de maintenir notre corps dans une position verticale et assurent la mobilité ainsi que la flexibilité de la colonne vertébrale.

Cendrillon Landolt : La Cendrille au corps d’Apollon <br>28 ans.

Oksana Orobets : Pour être toujours en bonne forme, il est essentiel d’aimer soi-même et son corps.
Articles recommandés
Plus de galeries
 Olga Gourieva est née le 18 novembre 1980 dans la ville de Iaroslavl.
Olga Gourieva est née le 18 novembre 1980 dans la ville de Iaroslavl. Les muscles du dos. Les muscles du dos nous permettent de maintenir notre corps dans une position verticale et assurent la mobilité ainsi que la flexibilité de la colonne vertébrale.
Les muscles du dos. Les muscles du dos nous permettent de maintenir notre corps dans une position verticale et assurent la mobilité ainsi que la flexibilité de la colonne vertébrale. Cendrillon Landolt : La Cendrille au corps d’Apollon <br>28 ans.
Cendrillon Landolt : La Cendrille au corps d’Apollon <br>28 ans. Oksana Orobets : Pour être toujours en bonne forme, il est essentiel d’aimer soi-même et son corps.
Oksana Orobets : Pour être toujours en bonne forme, il est essentiel d’aimer soi-même et son corps. Malheureusement, ce n’est pas tout le monde qui comprend correctement le concept de « tenue sportive ».
Malheureusement, ce n’est pas tout le monde qui comprend correctement le concept de « tenue sportive ».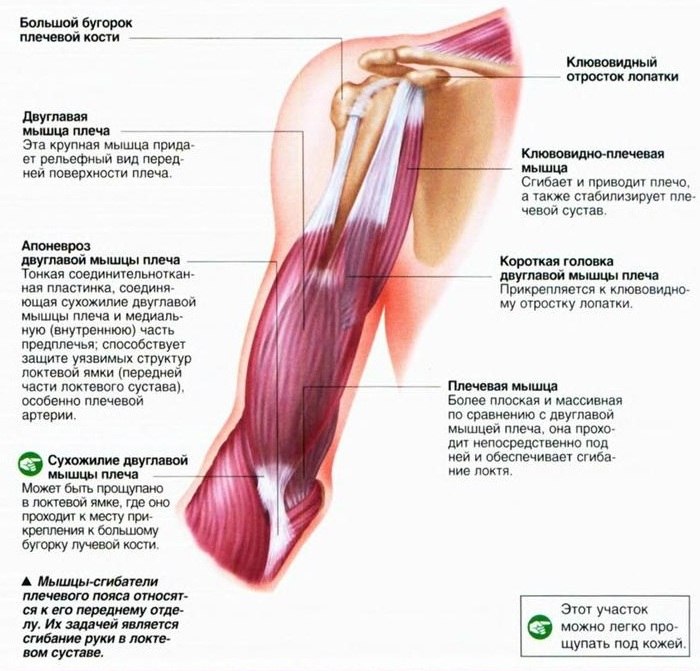 Les muscles de l’épaule. Les muscles de l’épaule peuvent être divisés en deux groupes distincts.
Les muscles de l’épaule. Les muscles de l’épaule peuvent être divisés en deux groupes distincts. Qui a essayé les nouveaux appareils d'exercice ?
Qui a essayé les nouveaux appareils d'exercice ? Résultats de Mr Olympia 2013.
Résultats de Mr Olympia 2013. Ashley Kaltwasser a remporté la 1ère place au compétition BIKINI OLYMPIA en 2013.
Ashley Kaltwasser a remporté la 1ère place au compétition BIKINI OLYMPIA en 2013. Il ne reste plus beaucoup de temps avant les Jeux Olympiques !
Il ne reste plus beaucoup de temps avant les Jeux Olympiques ! Ashley Horner, 29 ans. 50 kg pendant la saison<br>58 kg en dehors de la saison<br>164 cm.
Ashley Horner, 29 ans. 50 kg pendant la saison<br>58 kg en dehors de la saison<br>164 cm. Quand vous n’avez rien à faire, occupez-vous de vous-même.
Quand vous n’avez rien à faire, occupez-vous de vous-même.



